-
MagBeads®系列功能化磁珠在糖基化蛋白質及糖肽富集中的應用
發(fā)布時間: 2026-01-25 點擊次數(shù): 438次蛋白質糖基化是生命體內一種關鍵且普遍的翻譯后修飾,對細胞間通訊、信號傳導和免疫反應等眾多生物學過程至關重要。該修飾的異常與多種疾病(如神經退行性疾病和癌癥)的發(fā)生發(fā)展密切相關。值得注意的是,目前(FDA)批準的腫瘤標志物,如糖抗原199(CA19-9)、前列腺特異性抗原(PSA)和甲胎蛋白(AFP)等,絕大多數(shù)都屬于糖蛋白。此外,大量位于細胞膜或細胞外的糖蛋白(例如表皮生長因子受體-2/Her2作為乳腺癌治療靶點)已成為重要的藥物作用靶標。這些因素共同推動了蛋白質糖基化研究,使其成為跨越化學、生物學及臨床醫(yī)學等多學科的前沿交叉領域。
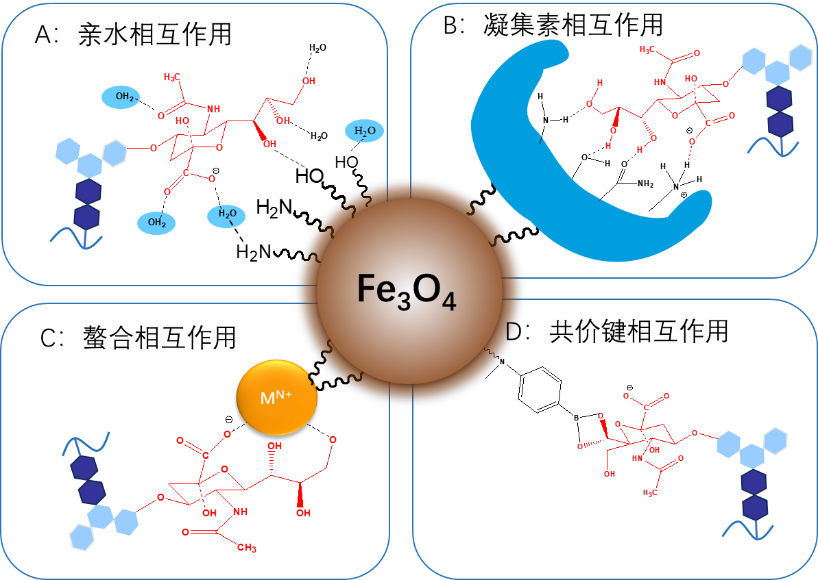
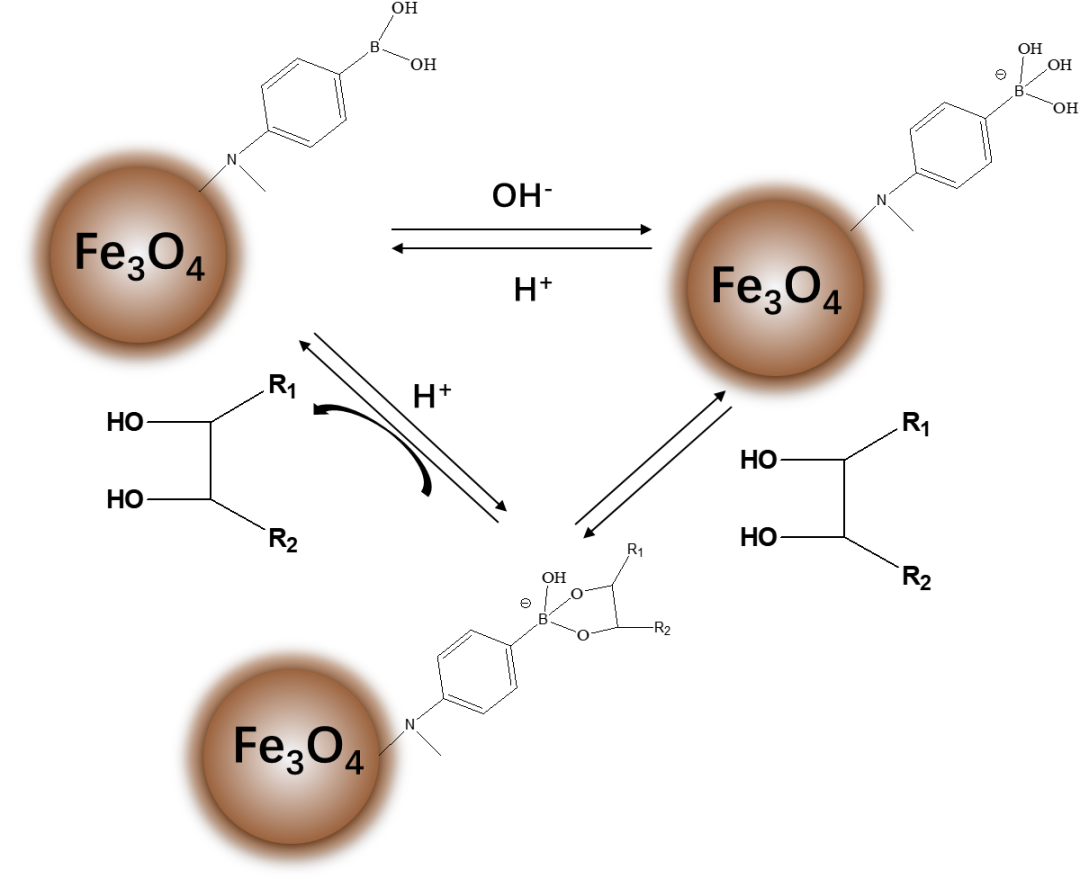
用于糖蛋白和糖肽富集的磁性微納米材料根據(jù)表面修飾的不同可分為基于親水性功能基團修飾、凝結素修飾、螯合作用修飾、共價作用修飾等方法。
總結
訂貨信息

參考文獻:
1. 高文杰, 等:功能化磁性納米材料在糖蛋白及糖肽富集中的研究進展,色譜,2021, 39 (9), 981-988.
2. 魯艷,等:分離富集磷酸化/糖基化蛋白質/肽的磁固相萃取新材料,分析測試學報, 2025, 44 (1), 1-11.
3. 鄧春輝, 陳和美, 磁性微納米材料在蛋白質組學中的應用,復旦大學出版社
?
END
?
產品中心
Products
-
血清系列
-
細胞轉染
-
支原體清除
-
細胞凍存
-
實驗耗材
-
分子試劑
-
細胞增殖與凋亡
-
Biozellen系列
-
培養(yǎng)基
-
ELISA試劑盒
-
TOYOBO(東洋紡)
-
ZYMO RESEARCH
-
Greiner(格瑞納)
-
IKA(艾卡)
-
化學發(fā)光底物(ECL)
-
PROSPEC系列
-
Epigentek系列
-
微生物檢測
-
細胞生物學
-
Corning康寧
-
解離試劑
-
細胞類-實驗耗材
-
原代細胞
-
植物檢測系列試劑盒
-
SERANA
-
細胞系
-
生化試劑盒
-
環(huán)境檢測系列試劑盒(AKEN)
-
類器官培養(yǎng)
-
緩沖器和解決方案
-
生物三凝膠基質
-
細胞因子分子
-
生物樣本庫
-
蛋白研究系列
-
修飾檢測試劑盒